【中文说明书】阿达格拉西布Adagrasib(KRAZATI)
- 相关药企 :Mirati / 米拉蒂治疗公司
- 说明书药企最新修订日期 :
- 说明书最新整理日期 :2024年2月
- 说明书其它说明 :-
【药品名称】
通用名:阿达格拉西布
英文名:Adagrasib
商品名:KRAZATI
【适应症】
KRAZATI适用于治疗患有KRAS G12C突变的局部晚期或转移性非小细胞肺癌(NSCLC)的成人患者,该患者已接受至少一次既往系统治疗,且已通过FDA批准的检测。
在基于客观缓解率(ORR)和缓解持续时间(DOR)的加速批准下批准了该适应症。对该适应症的持续批准可能取决于确认性试验中临床获益的验证和描述。
【剂量和用法】
患者选择
根据血浆或肿瘤标本中是否存在KRAS G12C突变,选择使用KRAZATI治疗局部晚期或转移性NSCLC的患者。如果血浆标本中未检测到突变,则检测肿瘤组织。
建议用量
KRAZATI的推荐剂量为600 mg,每日两次口服,直至疾病进展或出现不可接受的毒性。
KRAZATI,每日一次,与食物同服或不同服。整片吞下。请勿咀嚼、压碎或分裂药片。
如果服用KRAZATI后出现呕吐,则不要再服用一剂。在下次计划时间恢复给药。
如果无意中遗漏了某个剂量,则在距预期给药时间超过4小时时应跳过该剂量。在下次计划时间恢复给药。
不良反应剂量调整
表1列出了不良反应的建议减量。如果发生不良反应,最多允许减少两次剂量。对于无法耐受每日一次600 mg的患者,永久停用KRAZATI。
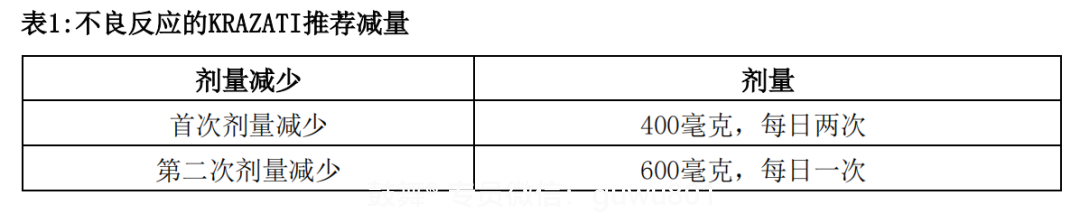
表2提供了不良反应的推荐剂量调整。
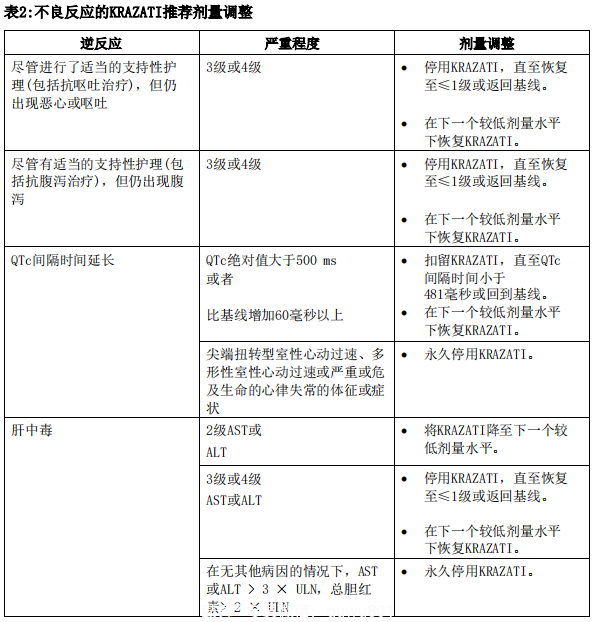
【警告和注意事项】
胃肠道不良反应
KRAZATI可引起严重的胃肠道不良反应。
在汇总的安全性人群中,观察到的严重胃肠道不良反应为胃肠道出血,占3.8%,其中0.8%为3级或4级,
胃肠道梗阻占1.6%,其中3级或4级占1.4%,结肠炎占0.5%,其中3级占0.3%,肠梗阻占0.5%,狭窄占0.3%。此外,366名患者中有89%发生恶心、腹泻或呕吐,其中9%为3级。恶心、腹泻或呕吐导致29%的患者中断给药或减少给药,0.3%的患者永久停用阿达格拉西。
根据指示,使用支持性护理(包括止泻剂、止吐药或补液)监测和管理患者。根据严重程度停用、减少剂量或永久停用KRAZATI。
QTc间隔时间延长
KRAZATI可导致QTc间期延长,从而增加室性快速性心律失常(如尖端扭转型室性心动过速)或猝死的风险。
在汇总的安全性人群中,在至少进行过一次基线后心电图(ECG)评估的366名患者中,6%的患者平均QTc ≥ 501 ms,11%的患者QTc > 60 msec的自基线升高。KRAZATI会导致QTc间隔时间出现浓度依赖性增加。
避免将KRAZATI与其他已知可能延长QTc间隔时间的产品同时使用,避免在先天性长QT综合征患者和QTc同时延长的患者中使用KRAZATI。
开始KRAZATI之前、合用期间以及充血性心力衰竭、缓慢性心律失常、电解质异常患者和无法避免已知会延长QT间隔时间的合用药物患者的临床指征下,监测ECG和电解质。根据严重程度,停用、减少剂量或永久停用KRAZATI。
肝中毒
KRAZATI可引起肝毒性,进而导致药物性肝损伤和肝炎。
在366名患者的汇总安全性人群中,0.3%的患者报告有药物性肝损伤,其中0.3%为3级。总计有32%接受阿达木昔布治疗的患者出现丙氨酸转氨酶(ALT)/天冬氨酸转氨酶(AST)升高;5%为3级,0.5%为4级。ALT/AST升高首次出现的中位时间为3周(范围:0.1至48)。总肝毒性发生率为37%,其中7%为3级或4级。12%的患者发生了导致剂量中断或减少的肝毒性。0.5%的患者因肝毒性停用Adagrasib。
在开始KRAZATI治疗前监测肝脏实验室检测(AST、ALT、碱性磷酸酶和总胆红素),每月一次,为期3个月或根据临床指示,对出现转氨酶升高的患者进行更频繁的检测。根据严重程度减少剂量、停用或永久停用KRAZATI。
间质性肺病/肺炎
KRAZATI可引起间质性肺病(ILD)/肺炎,可能致命。
在汇总的安全性人群中,4.1%的患者发生ILD/肺炎,1.4%为3级或4级,1例为致死性。ILD/肺炎首次发病的中位时间为12周(范围:5至31周)。0.8%的患者因ILD/肺炎停用阿达木。
在KRAZATI治疗期间,监测患者是否出现指示ILD/肺炎的新的或恶化的呼吸系统症状(如呼吸困难、咳嗽、发热)。在疑似ILD/肺炎患者中停用KRAZATI,如果未发现ILD/肺炎的其他潜在原因,则永久停用KRAZATI。
【药物相互作用】
其他药物对KRAZATI的影响
强CYP3A4诱导剂
避免将KRAZATI与强效CYP3A诱导剂联用。
Adagrasib是CYP3A4底物。与强效CYP3A诱导剂一起使用KRAZATI会降低adagrasib暴露量,这可能会降低KRAZATI的有效性。
强效CYP3A4抑制剂
避免将KRAZATI与强效CYP3A抑制剂合用,直至adagrasib浓度达到稳态(约8天后)。
Adagrasib是CYP3A4底物。如果adagrasib浓度未达到稳态,同时使用强效CYP3A抑制剂会增加adagrasib浓度,,这可能会增加KRAZATI不良反应的风险。
KRAZATI对其他药物的影响
敏感的CYP3A底物
除非这些底物的处方信息中另有建议,否则避免将KRAZATI与敏感的CYP3A底物联用。
Adagrasib是一种CYP3A抑制剂。与KRAZATI联合用药会增加CYP3A底物的暴露量,这可能会增加与这些底物相关的不良反应的风险。
敏感CYP2C9底物
除非这些底物的处方信息中另有建议,否则在最小浓度变化可能导致严重不良反应的情况下,避免将KRAZATI与敏感的CYP2C9底物联用。
Adagrasib是一种CYP2C9抑制剂。与KRAZATI联合用药会增加CYP2C9底物的暴露量,这可能会增加与这些底物相关的不良反应的风险。
敏感CYP2D6底物
除非这些底物的处方信息中另有建议,否则在最小浓度变化可能导致严重不良反应的情况下,避免将KRAZATI与敏感的CYP2D6底物联用。
Adagrasib是一种CYP2D6抑制剂。与KRAZATI联合用药会增加CYP2D6底物的暴露量,这可能会增加与这些底物相关的不良反应的风险。
P-gp基板
除非这些底物的处方信息中另有建议,否则在最小浓度变化可能导致严重不良反应的情况下,避免将KRAZATI与P-gp底物联用。
Adagrasib是一种P-gp抑制剂。与KRAZATI联合用药会增加P-gp底物的暴露量,这可能会增加与这些底物相关的不良反应的风险。
延长QTc间期的药物
避免将KRAZATI与其他已知可能延长QTc间隔时间的产品同时使用。如果不能避免合用,则在开始KRAZATI之前、合用期间和临床指示时监测心电图和电解质。如果QTc间隔时间> 500 ms或自基线的变化> 60 ms,则停用KRAZATI。
Adagrasib会导致QTc间隔时间延长。与延长QTc间隔时间的其他产品合用KRAZATI可能导致QTc间隔时间更长以及与QTc间隔时间延长相关的不良反应,包括尖端扭转型室性心动过速、其他严重心律失常和猝死。
【特定人群】
怀孕
风险汇总
没有关于孕妇使用KRAZATI的可用数据。在动物生殖研究中,在器官发生期间,当暴露量低于每日两次600 mg建议剂量的人体暴露量时,妊娠大鼠和兔口服阿达格拉西未引起不良发育影响或胚胎-胎仔致死性(参见数据)。
在美国普通人群中,临床确诊妊娠的重大出生缺陷和流产背景风险估计值分别为2%至4%和15%至20%。
数据-动物数据
在一项大鼠胚胎-胎仔发育研究中,在器官形成期间,每日一次对妊娠大鼠口服Adagrasib导致母体毒性(体重和食物摄入减少,以及导致濒死状态和早期终止的不良临床体征)和270 mg/kg剂量水平下的胎仔体重降低(基于体表面积,约为每日两次600 mg建议剂量的2倍[BSA])。Adagrasib诱导的骨骼畸形,如弯曲的肢体,和骨骼变异,如弯曲的肩胛骨,波浪状肋骨,和多生的短颈肋骨在270毫克/千克,这是继发于母体毒性和胎儿体重减少。
在一项兔胚胎-胎仔发育研究中,在器官形成期间每日一次口服阿达木昔布,在30 mg/kg剂量下(约为每日两次600 mg临床剂量下以曲线下面积[AUC]计算的人类暴露量的0.11倍)导致未分类胸骨的胎仔体重降低和产仔频率增加。这种骨骼变异与母体毒性有关,包括平均体重下降和食物消耗量减少。在每日一次剂量高达30 mg/kg的兔中,Adagrasib暴露未引起不良发育影响,也未影响胚胎-胎仔存活。
哺乳
风险汇总
没有关于adagrasib或其代谢产物在人乳中的存在、对母乳喂养的儿童的影响或对产奶量的数据。由于母乳喂养的儿童可能出现严重的不良反应,建议妇女在接受KRAZATI治疗期间以及末次给药后1周内不要进行母乳喂养。
具有生育能力的女性和男性
不孕
根据动物研究的结果,KRAZATI可能会损害具有生育能力的女性和男性的生育能力。
儿科使用
尚未确定KRAZATI在儿科患者中的安全性和有效性。
老年用药
在KRYSTAL-1接受每日两次adagrasib 600 mg口服给药的116名患者中,49% (57名患者)的年龄≥ 65岁。未观察到老年患者和青年患者在安全性或有效性方面的总体差异。
【临床药理学】
作用机理
Adagrasib是KRAS G12C的不可逆抑制剂,与KRAS G12C中的突变半胱氨酸共价结合,并将突变KRAS蛋白锁定在其非活性状态,从而在不影响野生型KRAS蛋白的情况下阻止下游信号传导。Adagrasib在含有KRAS G12C突变的细胞中抑制肿瘤细胞生长和存活,并在KRAS G12C突变的肿瘤异种移植模型中导致肿瘤消退,具有最小的脱靶活性。
药效学
Adagrasib暴露-反应关系和药效反应时间过程未知。
心脏电生理
Adagrasib以浓度依赖性方式增加QTc。基于浓度- QTcF关系,患者每日两次服用阿达格拉西b 600 mg后,平均稳态最大浓度(Cmax,ss)下的QTcF自基线的平均(90% CI)变化(δQTcF)为18 (15,21)ms。
【储存】
将药片储存在20°C至25°C(68°F至77°F)的室温下。允许15°C至30°C(59°F至86°F)的温度波动。
本站根据美国食品药品监督管理局(FDA)公布的信息,整合翻译各药物最新的中文说明,以供医生和患者参考,若有疑问之处,请联系我们,我们将及时进行确认和修正!