一线肝癌和 NSCLC!阿斯利康 PD-L1+ CTLA4 联合疗法获欧盟批准
来源:Insight 数据库
2 月 22 日,阿斯利康发布公告,PD-L1 单抗度伐利尤单抗(Imfinzi)、CTLA4 单抗替西木单抗(Imjudo)联合疗法 2 项适应症获欧盟批准:晚期或不可切除肝癌(HCC)成年患者的一线治疗,以及与化疗联用治疗 IV 期(转移性)非小细胞肺癌成人患者的治疗。
来自:阿斯利康官网
HCC 适应症的获批是基于 HIMALAYA III 期试验的积极结果。这是一项随机、开放标签、全球多中心 III 期临床,评估了 Imfinzi 单药、Imfinzi 联用 CTLA-4 单抗 tremelimumab 与索拉非尼相比一线治疗肝细胞癌的疗效。
Imfinzi 和 Imjudo 联合疗法使用被称为 STRIDE 方案的给药方式,单次给药 Tremelimumab(300mg)+ 高剂量 Imfinzi(1500mg),随后每 4 周一次给药 Imfinzi。
在 2022 ASCO GI 中,阿斯利康公布了 HIMALAYA 研究的最终数据。相较于索拉非尼组,接受 STRIDE 方案治疗的患者死亡风险降低了 22%(HR=0.78;96.02%[CI]:0.65-0.93,p=0.0035)。联合疗法组中位 OS 为 16.4 个月,而索拉非尼组为 13.8 个月。据估计,31% 接受联合疗法的患者在 3 年后仍然存活,而索拉非尼组这一数值为 20%。
HIMALAYA 研究疗效数据
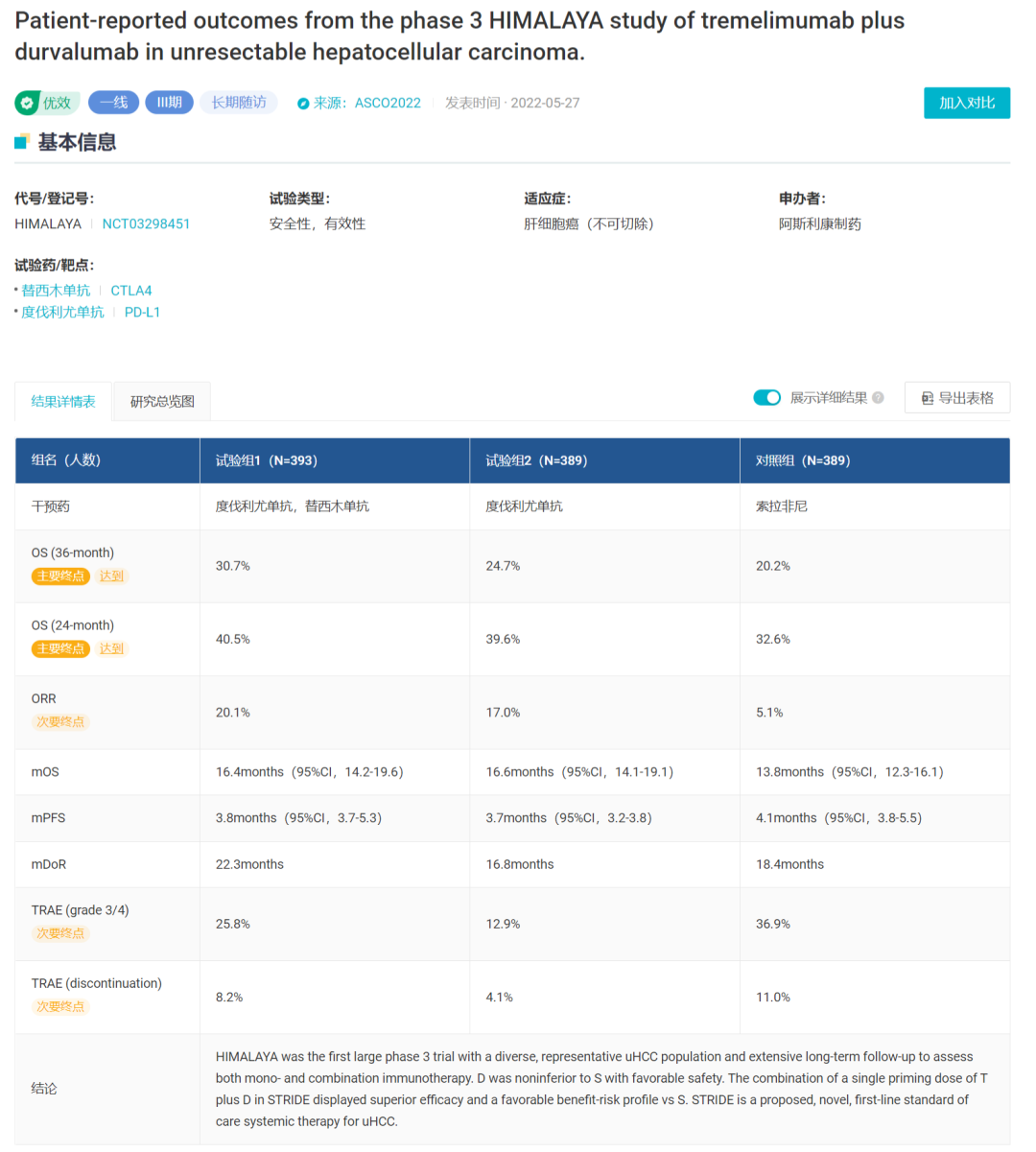
而获批 NSCLC 适应症是基于 III 期 POSEIDON 试验的结果。
与单独化疗相比,Imfinzi 联合四个周期的化疗中加入有限疗程的 Imjudo,可显著降低 23% 的死亡风险(HR=0.77;95% CI:0.65-0.92;p = 0.00304),中位 OS 为 14.0 个月,化疗为 11.7 个月。据估计,33% 接受该联合疗法的患者在两年内仍能存活,而化疗患者的存活率为 22%。
与单独化疗相比,这种联合治疗还降低了 28% 的疾病进展或死亡风险(HR=0.72;95% CI:0.60-0.86:p=0.00031),中位无进展生存期(PFS)分别为 6.2 个月和 4.8 个月。
POSEIDON 试验结果

在 2022 ESMO 大会上发布的 POSEIDON III 期临床试验的更新结果显示:
与单独化疗相比,在 Imfinzi 联合铂类化疗的基础上再联合 5 个周期有限疗程的 tremelimumab(Imjudo)可将总生存期提高 25%(HR=0.75;95% CI: 0.63-0.88)。联合治疗组更新的中位 OS 为 14 个月,而单独化疗组为 11.7 个月。接受联合治疗的患者中据估计有 25% 在三年时仍然存活,而这一比例在接受单独化疗的患者中仅为 13.6%。
POSEIDON 试验更新结果
