PARP抑制剂治疗小细胞肺癌进展
来源:希望树
PARP抑制剂作用机制
正常情况下,人体细胞产生的大量DNA单链断裂可通过PARP介导的碱基切除修复(BER)途径修复。DNA双链断裂的主要修复途径为非同源末端连接(NHEJ)修复和同源重组修复(homologous recombinant repair,HRR),前者速度快,但是会发生修复错误,导致基因组不稳定性。后者精确度高,修复后的DNA具有高保真性。PARP抑制剂正是利用“合成致死”机制杀伤肿瘤细胞,一方面通过抑制PARP酶催化活性和PARP捕获,使DNA单链断裂无法修复并大量堆积,进而产生大量的DNA双链损伤。同时,当细胞存在同源重组修复缺陷(homologous recombination deficiency,HRD)时,DNA双链断裂无法修复或者依赖容易错配的NHEJ途径修复,二者作用叠加,增加细胞死亡。
同源重组修复相关基因包括ATM,ATR,BARD1,BLM,BRCA1,BRCA2,BRIP1,CHEK2,MRE11A,NBN,PALB2,RAD51C,RAD51D,RBBP8,SLX4和XRCC2等,其中BRCA1/2基因突变是引起HRD最明确的HRR基因,也是迄今为止最理想的PARP抑制剂疗效预测标志物。但并不是所有HRR基因变异会导致HRD,对不同类型肿瘤的影响也有较大差异。
在转移性癌中,HRD的发生率为6%,其中在卵巢癌中的发生率(30%)最高,在乳腺癌、前列腺癌和胰腺癌中发生率(12%~13%)相当,而在其他肿瘤中少见;HRR相关基因突变频率为6%,以卵巢癌(30%~50%)和乳腺癌(12%~24%)最常见,其次是胰腺癌(7.3%~13.0%)和前列腺癌(5.3%~13.0%)。极少数小细胞肺癌患者会携带 RAD51D、CHEK1、BRIP1、BRCA1/2 等HRR相关基因胚系突变,可发生杂合性缺失(loss of heterozygosity,LOH),并可能对PARP抑制剂产生治疗应答。
现已上市的PARP抑制剂见表1。
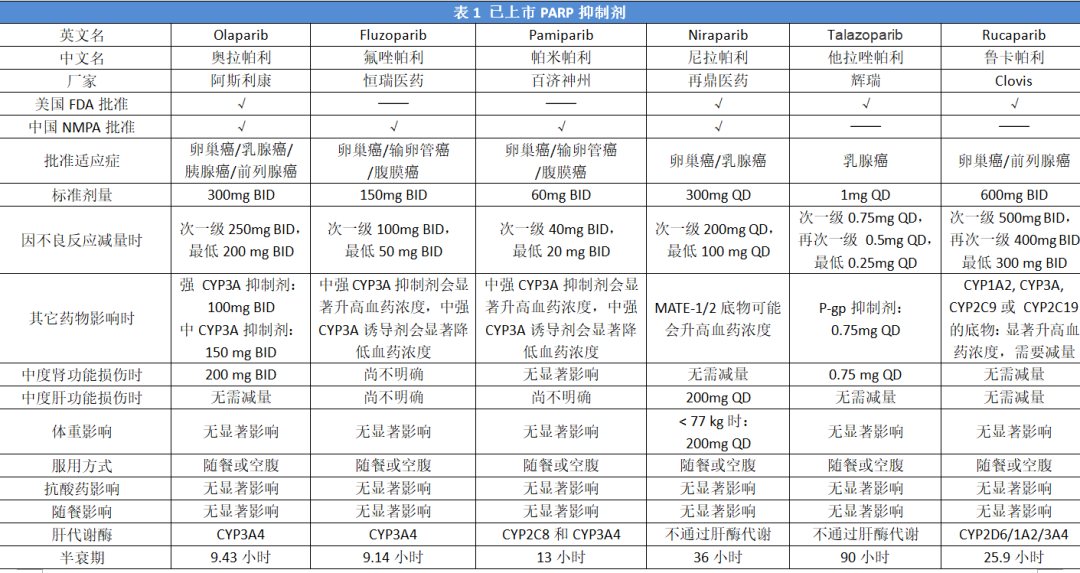
PARP抑制剂单药治疗SCLC
他拉唑帕利的一项一期研究(NCT01286987)中纳入了23例复发性SCLC患者,其中2例部分缓解,缓解持续时间3-4个月,4例疾病稳定,总有效率9%,中位无进展生存期11.1周。
奥拉帕利的一项二期研究(NCT03009682)中纳入了15例HRR基因变异的复发性SCLC患者,总有效率6.7%,疾病控制率26.7%,中位无进展生存期1.25月,中位总生存期8.56月。
广泛期SCLC患者一线含铂化疗后尼拉帕利维持治疗的三期研究(NCT03516084)没有达到临床终点,尼拉帕利组的中位无进展生存期1.54月(安慰剂组为1.36月),中位总生存期9.92月(安慰剂组为11.43月)。骨髓毒性是最常见的不良反应,其中贫血35.2%(3级以上5.6%),血小板减少37.6%(3级以上8%),白细胞减少31.2%(3级以上4.8%),中性粒细胞减少25.6%(3级以上9.6%)。
PARP抑制剂联合化疗治疗SCLC
Veliparib联合EP方案(依托泊苷和顺铂)一线治疗广泛期SCLC患者的二期研究(NCT01642251),总有效率71.9%(安慰剂组为65.6%),中位无进展生存期6.1月(安慰剂组为5.5月),中位总生存期10.3月(安慰剂组为8.9月)。
奥拉帕利联合替莫唑胺(Temozolomide,TMZ)治疗复发性/难治性SCLC患者的I/II期研究(NCT02446704),纳入了50例患者,86%PS 1分,72%铂类敏感,系统治疗史中位数2。
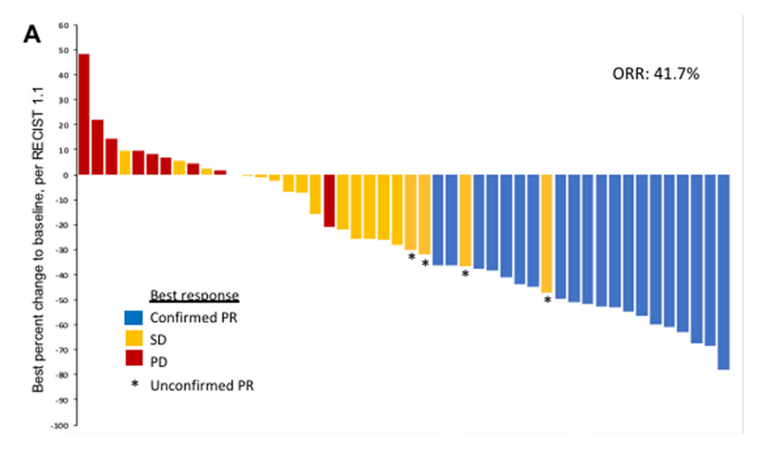
II期阶段,奥拉帕利200mg每天二次,替莫唑胺75mg/m2每天一次,均连续一周,然后停药二周,每三周一个疗程,总有效率41.7%,中位无进展生存期4.2月,中位总生存期8.5月。34例铂类敏感患者的总有效率47.1%,中位无进展生存期4.5月,中位总生存期9.4月;14例铂类抵抗患者的总有效率28.6%,中位无进展生存期2.9月,中位总生存期7.4月。最常见的不良反应为血小板减少(68%),贫血(68%),中性粒细胞减少(54%),疲劳(50%),恶心(42%)和呕吐(22%)。44%的患者减量,2例患者死于不良反应,分别为肺炎和中性粒细胞减少性败血症。
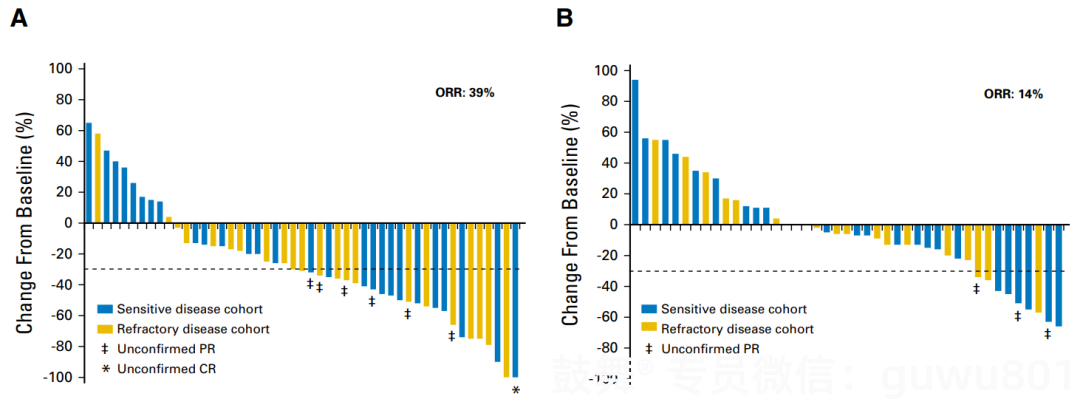
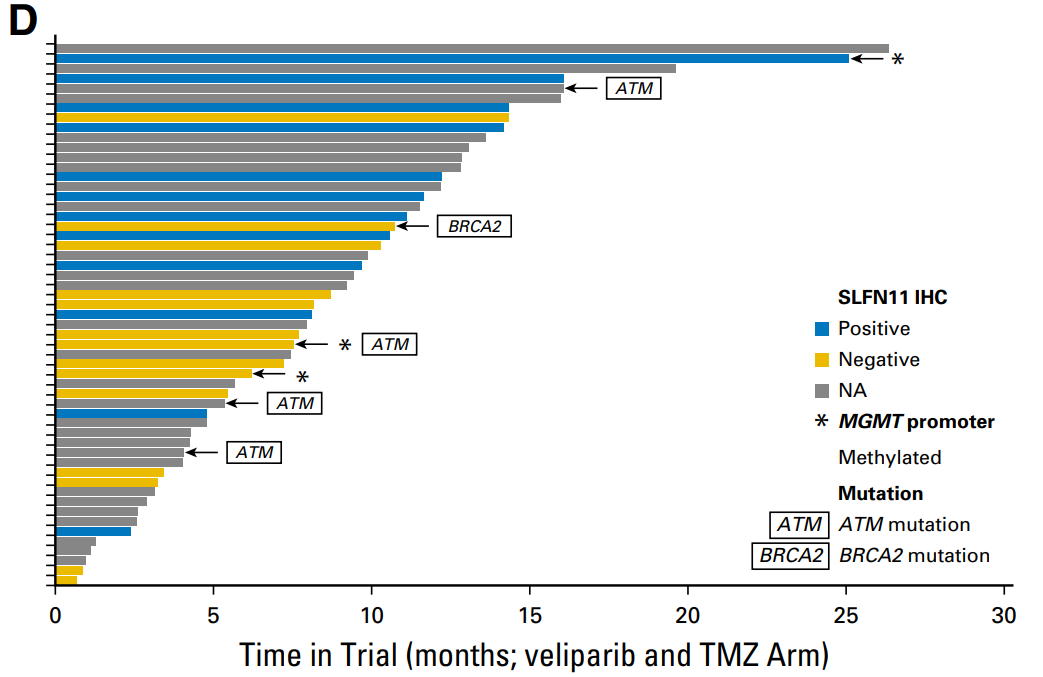
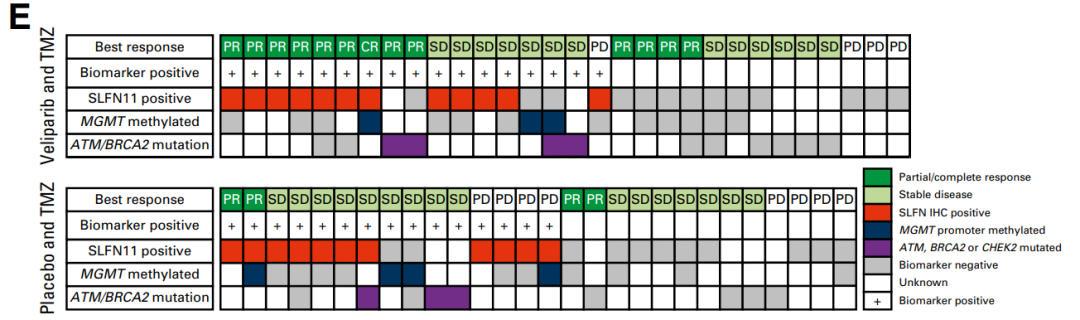
替莫唑胺单药或联合Veliparib治疗复发性SCLC患者的二期研究(NCT01638546),纳入了104例患者。Veliparib 40mg每天二次,连续一周,然后停药二周,替莫唑胺150-200mg/m2每天一次,连续5天,然后停药16天,每三周一个疗程。替莫唑胺联合Veliparib组的总有效率39%(替莫唑胺单药组为14%),中位无进展生存期3.8月(替莫唑胺单药组为2月),中位总生存期8.2月(替莫唑胺单药组为7月)。
替莫唑胺单药或联合组的常见3-4级不良反应均为骨髓毒性,贫血(2% Vs 11%),白细胞减少(7% Vs 24%),淋巴细胞减少(26% Vs 20%),中性粒细胞减少(7% Vs 31%),粒细胞减少性发热(0 Vs 34%)和血小板减少(27% Vs50%)。
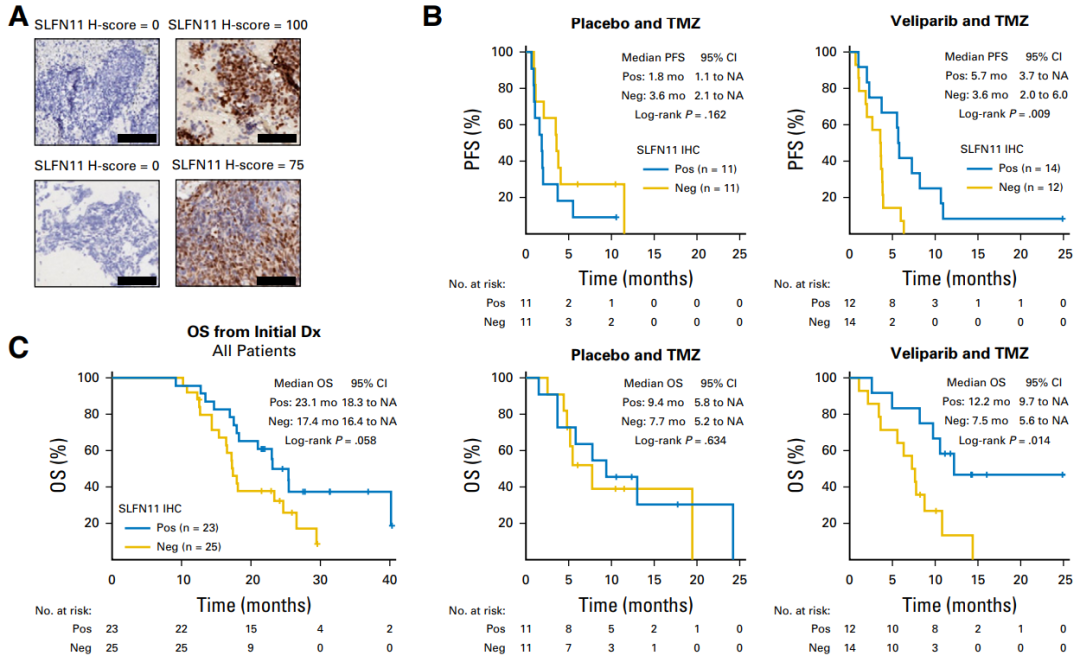
因SCLC患者中BRCA1/2突变罕见(比例小于2%),研究者采用IHC法测定的PARP-1和SLFN11表达作为疗效预测标志物。该研究中,没有发现PARP-1表达水平与临床疗效的相关性,而SLFN11表达阳性与联合组的临床疗效显著相关,中位无进展期5.7 Vs 3.6月,中位总生存期12.5 Vs 7.5月。
因联合方案的骨髓毒性较大,后续类似研究的方案设计采用了低剂量替莫唑胺。
尼拉帕利联合替莫唑胺维持治疗一线含铂化疗后缓解的SCLC患者的1b/II期研究(NCT03830918),尼拉帕利200mg每天一次,连续四周,替莫唑胺40mg每天一次,连续5天,每四周一个疗程,临床结果未出。
帕米帕利联合替莫唑胺治疗晚期实体瘤(包括复发性SCLC)的I/II期研究(NCT03150810),二期剂量为帕米帕利60mg每天二次,连续四周,替莫唑胺60mg每天一次,连续一周,然后停药三周,每四周一个疗程。最常见不良反应为恶心(46%,3-4级0),贫血(41%,3-4级1%),中性粒细胞减少(26%,3-4级21%)和血小板减少(27%,3-4级14%)。没有患者死于不良反应。剂量递增阶段共63例患者可供评估,总有效率14%,疾病控制率53%,中位缓解持续时间5.5月。
他拉唑帕利联合替莫唑胺二线治疗复发性SCLC患者的二期研究(NCT03672773),他拉唑帕利0.75mg每天一次(中度肾功能损伤患者0.50mg每天一次),连续四周,替莫唑胺37.5mg/m2每天一次,连续5天,每四周一个疗程。28例患者可供评估,总有效率39.3%,中位无进展生存期4.5月,中位总生存期11.9月。最常见3级以上不良反应为血小板减少(61.3%),贫血(54.8%),中性粒细胞减少(41.9%)和非典型性肺炎(3.2%)。
PARP抑制剂联合免疫治疗SCLC
奥拉帕利联合度伐利尤单抗二线治疗复发性SCLC的一项二期研究(NCT02484404),纳入20例患者,19例可供评估,1例BRCA1突变患者完全缓解,缓解时间已超过21个月,1例为EGFR突变腺癌转小细胞肺癌患者,缓解时间已超过5个月,另有2例疾病稳定超过8个月,总有效率10.5%,中位无进展生存期1.8月,中位总生存期4.1月。
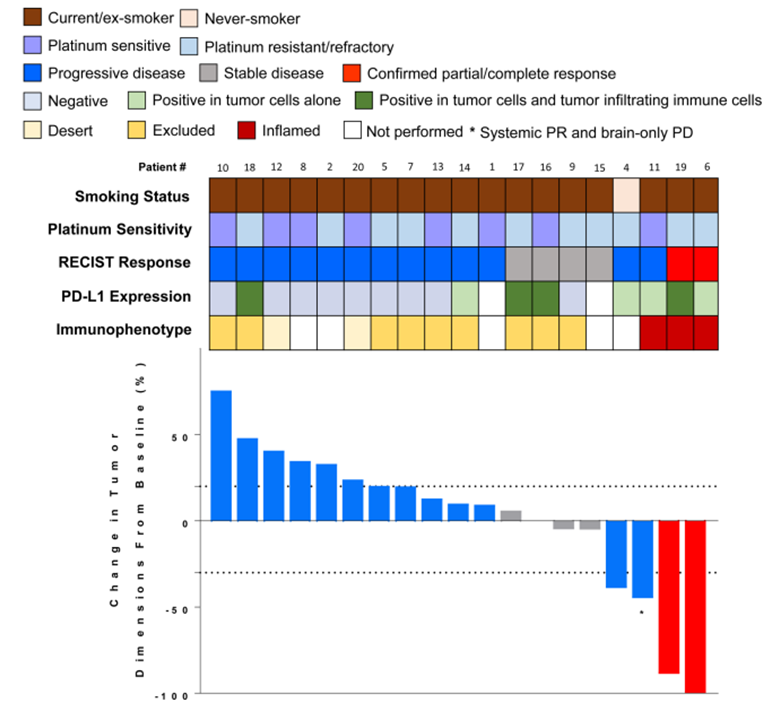
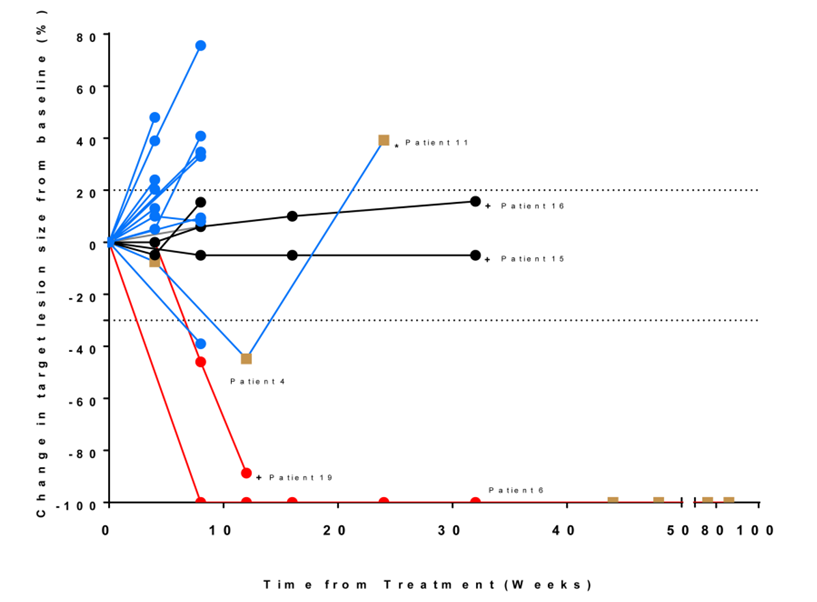
最常见的不良反应为贫血(80%),中性粒细胞减少(60%),白细胞减少(50%),疲劳(45%)和血小板减少(45%)。45%的患者发3-4级不良反应,1例患者因3级贫血减量,没有患者因不良反应停药。除有25%的患者发生无症状的促甲状腺激素升高外,没有发现神经和免疫毒性。
广泛期SCLC患者一线含铂化疗后,疗效评估为部分缓解或完全缓解的患者使用鲁卡帕利联合纳武利尤单抗维持治疗的二期研究(NCT03958045),中位无进展生存期2.67月,56%的患者有临床获益。
参考文献
DOI:10.3390/curroncol28010076
DOI:10.1007/s10637-020-01034-w
DOI:10.1007/s40262-022-01167-6
卵巢癌PARP抑制剂临床应用指南(2022版)
同源重组修复缺陷(HRD)临床检测与应用专家共识(2022版)
https://www.accessdata.fda.gov/drugsatfda_docs/label/2018/211651s000lbl.pdf(Talazoparib )
https://www.accessdata.fda.gov/drugsatfda_docs/label/2020/208447s015s017lbledt.pdf(Niraparib)
https://www.accessdata.fda.gov/drugsatfda_docs/label/2020/209115s004lbl.pdf(Rucaparib)
https://www.hengrui.com/uploads/20220111145544/f.pdf(氟唑帕利)
https://www.accessdata.fda.gov/drugsatfda_docs/label/2020/208558s014lbl.pdf(Olaparib)
DOI: 10.1038/bjc.2015.256
DOI:10.21037/jtd.2020.03.89
DOI:10.1200/JCO.2021.39.15_suppl.8562
DOI:10.1016/j.jtho.2021.04.001
DOI:10.1200/JCO.18.00264
DOI:10.1158/2159-8290.CD-19-0582
DOI:10.1016/j.jtho.2019.08.1135
DOI:10.1093/annonc/mdz244
DOI:10.1016/j.jtho.2019.04.026
DOI:10.1200/JCO.2022.40.16_suppl.8517
DOI:10.1016/j.jtho.2021.08.056
DOI:10.1200/JCO.2020.38.15_suppl.TPS908